出典:くらべてわかるできる子図鑑 p154
水溶液の種類3つ・特徴3つ・蒸発させると?速くとかす方法3つ
水溶液(酸性・中性・アルカリ性)と指示薬(リトマス紙・BTB・フェノールフタレイン)覚え方・語呂合わせ
中和の問題パターン2つ!完全中和点を探す系の問題は「逆比」で解く
水溶液と金属の反応(塩酸・水酸化ナトリウム)中性は金属が溶けない!
「金属と水溶液」と言っても、は~それで?という感じですよね?まず覚えるべきは、
●水溶液には金属を溶かすものと溶かさないものがある●
●金属も種類によって、溶けるものと溶けないものがある●
という事です。
そうすると当然、
「どういった水溶液はどういった金属を溶かすのか?」
「逆に金属を溶かさない水溶液は何なのか?」
「どんな金属がどんな水溶液に溶けないの?」
こういった点が試験上は問われそうですね?はい、問われます。
水溶液と金属の反応

出典:くらべてわかるできる子図鑑 p154
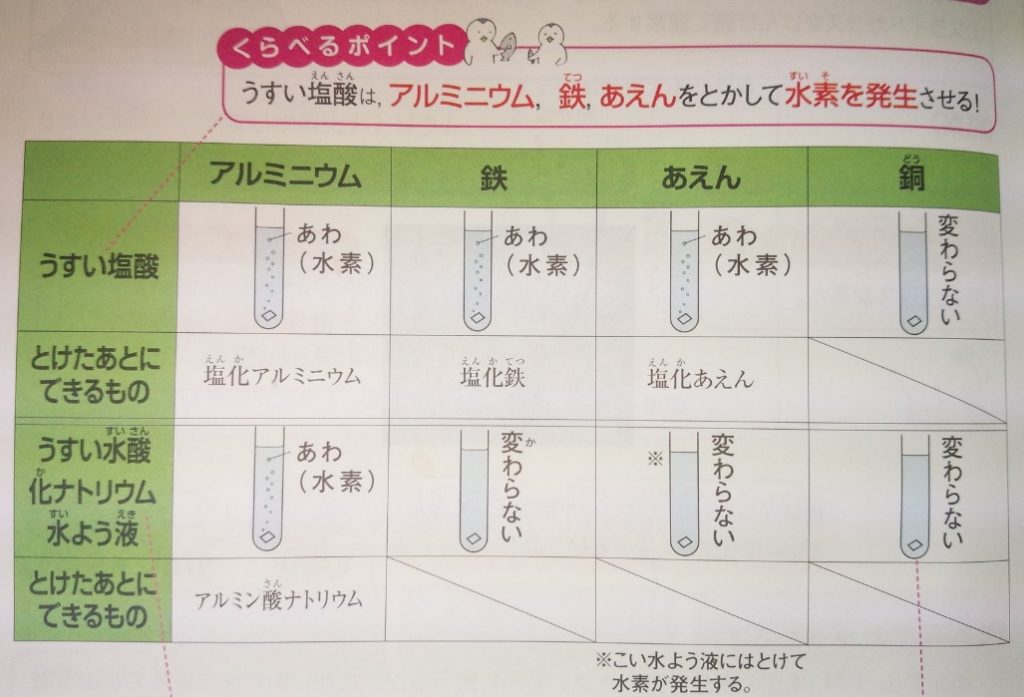
金属と水溶液の反応で使われやすい水溶液は、
●塩酸と水酸化ナトリウム●です。
また、溶ける金属は、
●水素●を出しながら溶けます。
~~~~~~~~~~~~~~~~~~~~~~~~
鉄+塩酸→塩化鉄+水素
アルミニウム+塩酸→塩化アルミニウム+水素
~~~~~~~~~~~~~~~~~~~~~~~

出典:くらべてわかるできる子図鑑 p154
塩酸に溶ける金属
【塩酸に溶ける金属:鉄・亜鉛・アルミニウム・マグネシウム】
鉄+塩酸→塩化鉄+水素
アルミニウム+塩酸→塩化アルミニウム+水素
水酸化ナトリウムに溶ける金属
【水酸化ナトリウムに溶ける金属:アルミニウム】
塩酸にも水酸化ナトリウムにも溶けない金属
【塩酸にも水酸化ナトリウムにも溶けない金属:金・銀・銅】
ポイント!塩酸と水酸化ナトリウムどちらにも溶けるのはアルミニウム

出典:くらべてわかるできる子図鑑 p154
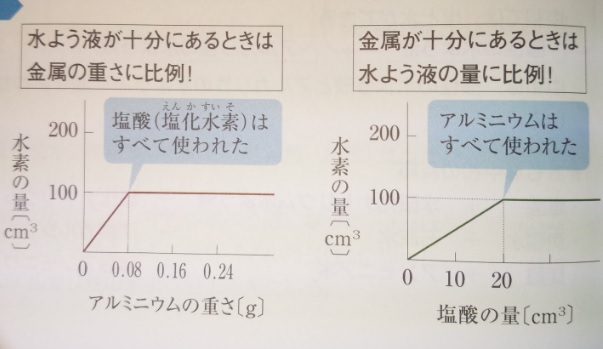
発生する水素の量は水溶液の量に比例
(濃度が一定なら)金属が溶けて発生する水素の量は、
金属の量や水溶液の量に比例する
出典:くらべてわかるできる子図鑑 p154
ポイントは、グラフが平らになるところです。この部分で、金属がなくなった
か、反応する水溶液がなくなり、水素が発生しなくなっています。
問題)上記のグラフでは、0.08gのアルミニウムに20c㎥の塩酸を加えると
水素が100c㎥発生する事がわかります。同じ塩酸で、2倍の水素(200c㎥)を
発生させるのに必要なアルミニウムは何c㎥ですか?
考え方)
金属が溶けて発生する水素の量は、
金属の量や水溶液の量に比例する
水素の量が2倍なら、必要なアルミニウムの量も2倍になります。
0.08×2=0.16
答え)0.16g
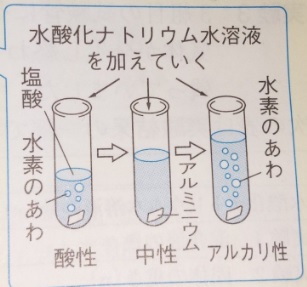
中性の水溶液に金属は溶けない
中性の水溶液に金属は溶けないので、逆に中和の進行を調べるために
使われる事があります。
画像出典『塾技100理科』p18
アルミニウムは塩酸にも水酸化ナトリウムにも溶けますので、
水素が発生せず、アルミニウムが溶けないのは完全中和の時
だけという事になります。
仮に、鉄を用いた場合、塩酸がある時は溶けますが、中和の
時と水酸化ナトリウムが余っているときは溶けません。
水溶液の種類3つ・特徴3つ・蒸発させると?速くとかす方法3つ
水溶液(酸性・中性・アルカリ性)と指示薬(リトマス紙・BTB・フェノールフタレイン)覚え方・語呂合わせ
中和の問題パターン2つ!完全中和点を探す系の問題は「逆比」で解く
水溶液と金属の反応(塩酸・水酸化ナトリウム)中性は金属が溶けない!